Les transferts
Trois phénomènes distincts sont à l'origine de la présence des produits phytosanitaires dans l'air. Soit les départs dans l'atmosphère se font dès les traitements, on parle de dérive (ou spray-drift), les gouttelettes les plus fines peuvent rester en suspension dans l'air et voyager sur de longues distances ; soit, leur présence dans l'air est due à l'érosion éolienne des sols traités (c'est-à-dire au transfert par le vent sous forme de particules de sols ou de poussières contaminées). Enfin, il est important de signaler l'existence de phénomènes plus complexes de transfert, sous forme gazeuse à partir des plantes ou du sol traités, la volatilisation.
Transfert vers l'atmosphère ou volatilisation
Le couvert végétal, la nature du sol, les conditions climatiques lors de l'application et les propriétés physico-chimiques des composés sont autant de facteurs qui influencent ces mécanismes et affectent par la même occasion les transferts de produits vers l'atmosphère. Ces différentes voies de passage des pesticides vers l'atmosphère peuvent impliquer des proportions variables des quantités de produits appliqués.
Une fois dans le compartiment aérien, les pesticides sont dégradés, principalement sous l'effet des rayonnements lumineux, mais ils peuvent néanmoins être transportés parfois sur de longues distances avant de retomber sous forme humide dans les pluies, les neiges ou les brouillards. L'atmosphère constituant une voie majeure pour le transport de ces composés dans l'environnement, il serait illusoire de penser que les régions d'agriculture intensive sont les seules concernées. Ainsi, ces polluants, qui voyagent par l'intermédiaire des mouvements des grandes masses d'air, vont pouvoir contaminer l'ensemble d'un territoire, y compris le milieu urbain.
Transferts vers les sols les eaux souterraines et les eaux de surface
Tôt ou tard, la plupart des pesticides arrivent sur le sol où ils sont soumis à un ensemble de mécanismes conditionnant leur devenir et leur dispersion vers les autres compartiments de l'environnement. Ces processus peuvent être biologiques ou abiotiques et concernent leur transformation (métabolisme par les microorganismes, photolyse, catalyse...), leur rétention (absorption par les végétaux ou la microflore du sol, et d'un certain nombre de processus physico-chimiques conduisant à la création de liaisons, plus ou moins réversibles, entre le pesticides et les constituants du sol) et leur transport (par les végétaux ou par la flore, par lixiviation, lessivage ou ruissellement ce qui pourra conduire à la contamination des eaux de drainage, des eaux de surfaces ou des nappes phréatiques).
La rétention
La rétention se réfère à la capacité du sol à retenir le pesticide et à en limiter le déplacement à l’intérieur ou à l’extérieur de la matrice du sol. Ce phénomène réduit alors temporairement le transfert des produits phytosanitaires vers l’eau et l’air. Pour les molécules non ionisées, la rétention augmente avec la teneur du sol en matière organique. Pour les autres molécules la rétention est plus difficile à estimer. Elle évolue cependant avec le temps et peut devenir quasi irréversible, produisant des résidus non extractibles appelés résidus liés.
La dégradation
La dégradation est la transformation du pesticide provoquant des modifications de la structure moléculaire avec apparition de métabolites. Ces transformations contribuent à diminuer la quantité de matière active dans le sol et donc à réduire les risques de pollution. Ainsi, dès leur application les pesticides subissent des processus biotiques ou abiotiques qui conduisent à leur dégradation plus ou moins complète. Ces mécanismes se produisent dans l’air, le sol, l’eau et les sédiments. Le principal processus de dégradation biotique des pesticides est assuré par les organismes biologiques de la microflore du sol (bactéries, champignons, algues, levures…), essentiellement dans les premiers centimètres du sol. La principale dégradation d’ordre physique (abiotique) est la photodécomposition par les rayonnements ultraviolets. Ce processus peut avoir lieu dans l’atmosphère, dans l’eau à la surface du sol et des plantes.
Des traitements répétés sur un sol avec un même pesticide peuvent aboutir à la sélection d’une microflore adaptée qui accélère la dégradation du pesticide appliqué.
La cinétique de dégradation d'une molécule donnée est déterminée en estimant la persistance du produit. Pour cela, on détermine sa demi-vie de dissipation (DT50) qui est la durée à l'issue de laquelle sa concentration initiale dans le sol a été réduite de moitié. Pour un même pesticide, la DT50 peut donc varier en fonction du pédoclimat et de l’activité microbiologique du sol. La minéralisation du pesticide, avec la transformation du carbone organique en CO2, est le processus ultime de dégradation et il est le seul provoquant une élimination complète du pesticide.
Le cas particulier du chlordécone
Le chlordécone fut breveté en 1952 aux Etats-Unis, le produit fut distribué par la société Dupont de Nemours à partir de 1958 sous le nom commercial de Kepone® ou de GC-1189® . Environ 55 formulations différentes furent mises sur le marché. Entre 1952 et 1975, environ 1 600 tonnes de Képone® furent produites aux Etats-Unis, dont l’essentiel de la production fut exporté en Asie, en Europe, en Amérique latine et en Afrique. Utilisé sous la forme d'une poudre à épandre concentrée à 5 % de chlordécone, le produit était utilisé pour la culture des bananes, du tabac et des agrumes.
Il semble qu’une part importante du chlordécone fabriqué aux Etats-Unis ait également été exportée vers la République Fédérale d’Allemagne où il a servi de base pour la fabrication du Kelevan® . Obtenu par condensation du chlordécone avec l’éthyl levulinate, le kelevan se dégrade dans le sol en libérant du chlordécone. Le Kelevan® a été utilisé surtout comme insecticide pour le contrôle du doryphore de la pomme de terre en Europe de l’Est et en Irlande mais il a servi également comme moyen de lutte contre le charançon du bananier et contre d’autres charançons des betteraves et du maïs. D'autre part, le Mirex® (perchlordécone) chimiquement très proche du chlordécone a également été utilisé aux Antilles françaises pour lutter contre la fourmi manioc ravageur des cultures vivrières (manioc, igname, patates douces...) et fruitières (oranges, citroniers, ananas). Cet appât, commercialisé en granules était déposé à l'entrée du nid, ce dernier étant rebouché après l'opération.
Après le passage des cyclones Allen en 1979 et David en 1980, les planteurs antillais se trouvaient démunis face à une pression parasitaire extrêmement forte. Le Curlone®, nouvelle formulation commerciale à base de chlordécone, était alors autorisé en 1981. Le Curlone® se présentait sous la forme d’une poudre pour poudrage à une concentration maximum de substance active de 5 %. Il était appliqué directement à raison de 30 g par pied de bananier, soit 1,5g de matière active, en deux applications préconisées chaque année, mais il était possible d’espacer les applications de 18 mois avec encore une bonne efficacité. Chaque application apportait ainsi 3 kg de chlordécone à l’hectare.
Le chlordécone fait partie des polluants organiques persistants inscrits dans la convention de Stockholm . Il appartient à la famille des organochlorés et présente les principales propriétés physico-chimiques de ce groupe de composés. Il est lipophile, peu soluble dans l’eau avec un faible potentiel de volatilisation. Il n’est ni hydrolysable, ni biodégradable dans l’environnement et sa photodégradation directe est infime. Dans les sols et les sédiments, le processus primaire de décomposition du chlordécone est la biodégradation anaérobique. Cependant, cette dégradation demeure très faible (moins de 10 %).
Ses propriétés physicochimiques en font une substance très stable qui se dégrade difficilement dans l’environnement. Le chlordécone retenu par les matières particulaires (poussières, sols et sédiments) et par les matières organiques se diffuse alors lentement dans les milieux et est entrainé dans les eaux de percolation et de ruissellement. Cet entraînement provoque également une contamination des rivières et des eaux souterraines. A la surface de l’eau ou dans l’air le chlordécone lié à des particules peut-être transporté sur de grandes distances.
Du fait de ses propriétés lipophiles, le chlordécone a une forte capacité à s’accumuler et à se bioconcentrer le long des chaînes alimentaires aquatiques, animales et végétales.

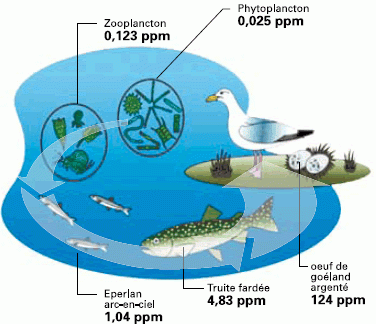
Source : US Environmental Protection Agency (1 ppm = 1mg/kg ou 1mg/L)
Phénomènes de bioconcentration, de bioaccumulation et de bioamplification
La bioconcentration est le processus par lequel les organismes vivants, en particulier ceux qui vivent dans l’eau, peuvent extraire et concentrer certaines substances chimiques de l’environnement qui les entourent. Ce phénomène est mesuré par le facteur de bioconcentration (BCF). Le BCF est le ratio entre la concentration du composé étudié dans le milieu (eau par exemple) et la concentration dans l'organisme.
La bioaccumulation est le même processus que la bioconcentration mais, en plus des apports directs des milieux, il intègre également les apports indirects par le biais de la nourriture.
La bioamplification ou biomagnification désigne l'augmentation cumulative, à mesure qu'on progresse dans la chaîne alimentaire (chaîne trophique), des concentrations d'une substance persistante. Ainsi, comme le montre le schéma ci-dessus, le polluant s'accumule à chaque étape de la chaîne alimentaire avec à son sommet (oeuf de goéland argenté) des concentrations de polluant persistant parfois 10000 fois supérieures à celle mesurée au niveau du premier maillon (phytoplancton).
Des concentrations plus élevées qu’en Martinique ont été mesurées en Guadeloupe sur les 30 premiers centimètres de sol. Ces différences de concentration s’expliquent par un échantillonnage important de sols de bananeraies pérennes en Guadeloupe non labourées depuis plusieurs décennies. Le chlordécone reste ainsi concentré dans les couches superficielles. La totalité des analyses réalisées pour la Martinique ont quand à elles été réalisées sur des sols ayant autrefois subi des labours profonds (60–70 cm). Le chlordécone ayant ainsi été dispersé au-delà des 30 premiers centimètres.
Cette substance présente dans le sol et les eaux des Antilles françaises est également retrouvée dans certains produits alimentaires d’origine végétale et animale. Les végétaux les plus fréquemment contaminés sont les légumes racines (patate douce, chou caraïbe, dachine, igname, carotte …). Cette contamination s’opère par migration directe du chlordécone présent dans le sol vers la racine. Ce transfert se fait à des taux très variables en fonction de paramètres qui restent encore à déterminer. Cependant la nature du sol et sa capacité à fixer la molécule semblent jouer un rôle majeur. Les fruits et les légumes de la famille des cucurbitacées (concombres, melon, pastèques, giraumon…) en contact avec la terre ou dont les parties comestibles sont proches de la racine peuvent également être contaminés. La fréquence et les niveaux de contamination sont cependant plus faibles que pour les légumes racines. Enfin, certaines études indiquent que les denrées végétales autres que celles citées précédemment, peuvent contenir du chlordécone par transport passif de la molécule dans les parties aériennes des végétaux.
Outre sa capacité à s’accumuler dans les plantes, du fait de son affinité pour les lipides, le chlordécone présente un fort potentiel de bioaccumulation dans les organismes aquatiques. Les processus de dégradation sont faibles ou quasi nuls dans les organismes exposés. Ainsi des facteurs de bioconcentration supérieurs à 60 000 ont été mesurés chez une espèce de poisson vivant dans les estuaires (capucette de l’atlantique). Les produits de la pêche et les produits d’eau douce peuvent donc être contaminés. Les animaux terrestres peuvent également être contaminés par ingestion d’aliments issus de zones ou le sol contient du chlordécone .